نصيحة 1: كيفية حل المشاكل في الكيمياء الصف 8
نصيحة 1: كيفية حل المشاكل في الكيمياء الصف 8
في معظم الحالات ، الحاضر أو السابقهناك على الأقل بعض الأفكار النظرية حول العمليات الكيميائية. لكن حل المشكلة في الكيمياء هو موقف صعب إلى حد ما ، إذا لم تكن هناك مهارات محددة. لكن المهمة الكيميائية هي المساعدة في المطبخ مع التخفيف ، على سبيل المثال ، من الجوهر الخالي أو مجرد تلميح ودية لابنك الصغير أو أختك الصغيرة. دعونا نتذكر كيفية حل المشاكل في الكيمياء؟ عادة ، في الصف الثامن ، تكون المهام الأولى باستخدام معادلات التفاعلات الكيميائية من النوع "حساب كتلة أحد منتجات التفاعل وفقًا للكتلة المعروفة لأحد المواد المتفاعلة". يتم حل المشكلة بمساعدة الصيغ الكيميائية ، لأنه في كثير من الأحيان في مهام الاستخدام هذه الطريقة مطلوبة.

تعليمات
1
المهمة. حساب كتلة من كبريتيد الألومنيوم إذا دخلت 2.7 غرام من الألومنيوم التفاعل مع حامض الكبريتيك.
2
نحن نكتب شرطًا مختصرًا ، ونعطى: m (Al) = 2، 7 gH2SO4 Find: m (Al2 (SO4) 3) -؟

3
قبل حل المشكلات في الكيمياء ، نشكلمعادلة التفاعل الكيميائي. عندما يتفاعل فلز مع حمض مخفف ، يتشكل الملح ويتم تحرير مادة غازية ، وهي الهيدروجين. نرتب المعامل2Al + 3H2SO4 = Al2 (SO4) 3 + 3H2. عند حل المشكلة ، يجب على المرء أن يهتم دائمًا فقط بالمواد التي يعرف المعروف عنها ، وكذلك العثور على المعلمات. كل ما تبقى لا تؤخذ بعين الاعتبار. في هذه الحالة ، ستكون: Al و Al2 (SO4) 3

4
نجد الكتل الجزيئية النسبية لهذهمن المواد وفقا لجدول مندليف ، نضع هذه القيم في الكتل المولية (M) ، بضربها بـ 1r / mol M (Al) = 27 g / mol M (Al2 (SO4) 3) = 342 g / mol

5
نكتب الصيغة الأساسية التي ترتبط بكمية المادة (n) والكتلة (m) والكتلة المولية (M) .n = m / M. نحسب المعادلة بالصيغة (Al) = 2.7 g / 27 g / mole = 0.1 mole

6
نحن نصنع علاقتين. تتكون العلاقة الأولى من المعادلة على أساس المعامِلات قبل صيغة المواد التي تعطى معلمات أو ينبغي العثور عليها: النسبة الأولى: 2 mol Al هي 1 mol Al2 (SO4) 3 النسبة الثانية: 0.1 mol is x mol Al2 (SO4) ) 3 (تم تجميعها من الحسابات) حل هذه النسبة ، مع الأخذ في الاعتبار أن X هي مقدار Al2 (SO4) 3 ولديها وحدة قياس mol. Hencen (Al2 (SO4) 3) = 0.1 مول (Al) • 1 مول (Al2) SO4) 3): 2 مول = 0.05 مول

7
الآن هناك كمية من المادة و الموليوبالتالي ، يمكننا العثور على الكتلة التي نستنتجها من الصيغة الأساسية: m = nMm (Al2 (SO4) 3) = 0.05 mol • 342 g / mole = 17.1 g الكتابة: m (Al2 (SO4) 3) = 17.1 جم

8
للوهلة الأولى ، يبدو أن حل مشاكلالكيمياء صعبة للغاية ، ولكنها ليست كذلك. وللتحقق من درجة إتقان هذا ، حاول أولاً أن تحل المشكلة نفسها ، لكن نفسك فقط. ثم استبدل القيم الأخرى باستخدام نفس المعادلة. والخطوة الأخيرة والنهائية هي حل المشكلة بالمعادلة الجديدة. وإذا تمكنت من التأقلم ، فما الذي يمكن أن نهنئك!
نصيحة 2: كيفية حل المشاكل باستخدام المعادلات
المهام يمكن دائما حلها مع مساعدة بطريقتين - من خلال الإجراءات والمعادلات. حل مشكلة الإجراءات في بعض الحالات هو أبسط من المعادلة، ولكن هناك أوقات عندما لا يمكن حل المشكلة من خلال الإجراءات. لهذا، يتم استخدام المعادلات.

تعليمات
1
أولا، في المهمة التي تريد حلها مع مساعدة المعادلات، يجب تحديد مصدر البيانات. على سبيل المثال: "سيارتين قاد في وقت واحد تجاه بعضهم البعض من نقطة A و B. سرعة سيارة واحدة - 60 كم / ساعة، والثانية - 50 كم / ساعة التقيا بعد 2 ساعة بعد مغادرة كم كيلومترا هي المسافة بين هذه النقاط .. ؟ " البيانات الأولية هنا هي سرعة كل جهاز والوقت الذي كانوا يستقلونها تجاه بعضهما drugu.Nam نحن بحاجة إلى اتخاذ كمية غير معروفة، وتعريفها ل x. هنا x هي المسافة بين النقاط.
2
الآن يجب علينا التعبير عن x من خلال المتبقيقيمة. هنا لدينا x = (60 + 50) * 2. نضيف سرعات كل من الآلات وتضاعف من قبل عدد الساعات التي قضاها في الوقت قبل الاجتماع. من هذا نجد X والكتابة في الجواب: "المسافة بين النقاط A و B هي 220 كم.
3
كما يمكنك الحصول على المهام أكثر صعوبة، فيوالتي س يعبر عنها في حالتين. على سبيل المثال: "اشترينا 5 كجم من التفاح و 4 كجم من الكمثرى.ومن المعروف أن كيلو من الكمثرى يكلف 12.5 روبل more.The تكلفة الشراء كلها 400 روبل.ما هي تكلفة كيلوغرام من الكمثرى والكيلوغرام من التفاح؟" هنا نحن التعبير عن كيلوغرام من التفاح من خلال x، و كيلوغرام من الكمثرى على التوالي من خلال x + 10. نحصل على المعادلة: 5x + 4x + 50 = 400. حلها والحصول على هذا كيلوغرام من التفاح يكلف 50 روبل، و كيلوغرام من الكمثرى - 60 روبل. نكتب الجواب وفقا لحالة المشكلة.
نصيحة 3: كيفية حل المشاكل على النسب
لا يترك أي شك في ذلك نسب - الشيء الذي تحتاجه. النسب في حياتنا في كل مكان. حساب الراتب للسنة ، مع معرفة الدخل الشهري. كم لشراء منتج مقابل المال ، إذا كان السعر معروفًا. كل شيء نسب.

تعليمات
1
عند حل المشاكل على نسب يمكنك دائما استخدام نفس المبدأ. هذا مريح. عند التعامل مع نسبة ، دائما التصرف بالترتيب التالي: تحديد المجهول وتعيينه بالحرف x.
2
اكتب الشرط المهام في شكل جدول.
3
تحديد نوع الاعتماد. يمكن أن تكون مباشرة أو عكسية. كيفية تحديد طريقة العرض؟ إذا كانت النسبة خاضعة للقاعدة "كلما كان ذلك أكثر ، كلما كان" ، فإن الاعتماد يكون مباشرًا. إذا كان على العكس ، "كلما كان ذلك أقل" ، ثم العلاقة العكسية.
4
ضع الأسهم على حواف جدولك وفقًا لنوع التبعية. تذكر: السهم يشير إلى الأعلى.
5
باستخدام الجدول ، وجعل نسبة.
6
تقرر هذه النسبة.
7
الآن دعونا ننظر إلى أمرين من نوع مختلفالتبعية.المشكلة 1. 8 قماش arshin يكلف 30 روبل. كم تبلغ 16 قطعة من هذه القماش؟ 1) غير معروف - تكلفة 16 قطعة قماش. نحن نقترحه بواسطة x.2) نحن نصب الجدول: 8 arshin 30 p.16 arshin x p.3) تحديد شكل الاعتماد. نحن نجادل كما يلي: كلما اشترينا قطعة قماش ، كلما دفعنا أكثر. وبالتالي ، فإن الاعتماد مباشر .4) نضع الأسهم في الجدول: ^ 8 arshin 30 r. ^ | 16 arshins x r. 5) سنؤلف النسبة: 8/16 = 30 / xx = 60 r الجواب: تكلفة 16 arshins من القماش 60 r.
8
المهمة 2. لاحظ السائق أنه بسرعة 60 كم / ساعة عبر الجسر عبر النهر لمدة 40 ثانية. في طريق العودة ، عبر الجسر في 30 ثانية. تحديد سرعة السيارة في طريق العودة 1) غير معروف - سرعة السيارة في طريق العودة 2) دعونا تجميع الجدول: 60 كم / ساعة 40 كم / ساعة 30 ث 3) تحديد شكل العلاقة. كلما ازدادت سرعة السيارة ، سرعان ما يمرر السائق الجسر. وبالتالي ، فإن الاعتماد معكوس 4) سنشكل النسبة. في حالة وجود علاقة عكسية ، هناك خدعة صغيرة هنا: يجب قلب أحد أعمدة الجدول. في حالتنا ، سيتم الحصول على النسبة التالية: 60 / س = 30 / 40x = 80 كم / ساعة: سافر السائق على طول الجسر بسرعة 80 كم / ساعة.
نصيحة 4: كيفية حل المشاكل في الكيمياء
القدرة على حل المشاكل في الكيمياء يمكن أن تكون مفيدةليس فقط طالب وطالب ، ولكن أيضا عامل في مكان العمل ، ربة منزل في المطبخ ، بستاني في الحديقة. هناك خوارزمية بسيطة تسمح بحل المشاكل الكيميائية القياسية.

سوف تحتاج
- المعرفة النظرية للكيمياء على مستوى المدرسة.
تعليمات
1
يجب معالجة حل المشكلة الكيميائيةمنهجي. تفكيك حالتها بعناية ، اكتب كل البيانات في العمود. نقل جميع القيم في نظام قياس واحد. قم بتدوين القيمة المطلوبة بشكل منفصل. يوضح الشكل 1 القيم المستخدمة في المهام المدرسية القياسية ووحدات القياس الخاصة بها.
2
أبسط نوع من المشاكل هو المشكلة التي تحلهابعض الصيغ الحسابية. في مثل هذه المشاكل ، ليس من الضروري صياغة معادلات التفاعل. يكفي أن ننظر عن كثب إلى جدول المعادلات الكيميائية القياسية (الشكل 2) ، واختيار تلك الصيغ التي ستكون مطلوبة للعثور على القيمة المطلوبة من البيانات المعروفة.
3
أكثر تعقيدا هي المهام التي فيهاالكواشف، وفي هذه الحالة تحتاج إلى إجراء سوف معادلة الرد سيكون المعرفة النظرية اللازمة عن التفاعلات الكيميائية الأساسية والمركبات من أجل تثبيت منتجات التفاعل بشكل صحيح. وبالإضافة إلى ذلك، سوف تكون هناك حاجة لتحقيق المساواة وينبغي أن نتذكر الأسعار في معاملات معادلة uravnenii.Dlya أن كمية كل مادة، كان رد فعل والمبلغ الإجمالي للمادة يبقى postoyannymi.Posle كيف سوف تجعل المعادلة رد فعل، وسوف تحتاج إلى العثور على عدد من المواد المعروفة، و ثم مع مساعدته كمية من مادة مجهولة. يقلل الحل الإضافي مرة أخرى إلى اختيار صيغة للعثور على الكمية المرغوبة.
4
هناك نوع من المشاكل الكيميائية فيالفائض / نقص. في هذه المشاكل ، من الضروري حساب كميات المواد المتفاعلة ومراعاة معاملات التفاعل لمعرفة أيهما أكبر. يجب إجراء المزيد من الحسابات على مادة أصغر ، لأنها ستتفاعل تمامًا ، ولكن المادة الزائدة ستبقى غير متفاعلة جزئيًا.
5
يمكن لأي شخص أن يتعلم حل المشاكل الكيميائية القياسية ، ويقول المعلمون إنه من الضروري حل حوالي 15 مهمة من كل نوع بشكل مستقل من أجل حلها بثقة.
نصيحة 5: كيفية حل المشاكل مع المعلمات
حل مشكلة مع معلمة يعني العثور على مايكون المتغير مساويا لأي قيمة أو قيمة محددة للمعلمة. بدلا من ذلك، يمكن أن تكون المهمة للعثور على تلك القيم المعلمة التي يفي المتغير شروط معينة.

تعليمات
1
إذا كانت المعادلة أو عدم المساواة تعطى لكتكون مبسطة، تأكد من استخدام هذا. تطبيق الأساليب القياسية لحل المعادلات، كما لو كانت المعلمة عدد عادي. ونتيجة لذلك، يمكنك التعبير عن المتغير من خلال معلمة، على سبيل المثال، x = p / 2. إذا كان في حل المعادلة لم تواجه أي قيود على قيمة المعلمة (أنها لا تقف تحت علامة الجذر، تحت علامة اللوغاريتم، في المقام)، كتابة هذه الإجابة، مشيرا إلى أنه تم العثور على جميع القيم الحقيقية للمعلمة ص.
2
لحل المشاكل مع الرسوم البيانية القياسية(على سبيل المثال، خط مستقيم، و القطع المكافئ، و هايبيربولا)، استخدم طريقة رسومية. تقسيم مجموعة القيم المعلمة إلى فترات تختلف فيها قيمة المتغير (أو المتغيرات)، ولكل فاصل زمني، إنشاء جزء من الرسم البياني. إيلاء اهتمام خاص إلى النقاط القصوى للخطوط - لتحديد بدقة انتمائهم إلى الرسم البياني، واستبدال هذه القيمة في وظيفة وحل المعادلة معها. إذا لم يكن للمعادلة حل في هذه المرحلة (على سبيل المثال، يتم الحصول على تقسيم من الصفر)، استبعاده من الرسم البياني عن طريق وضع علامة عليه مع دائرة فارغة.
3
لحل مشكلة فيما يتعلق معلمة،أولا، أخذ المتغير والمعلمة للمساويات في المعادلة أو عدم المساواة وتبسيط التعبير قدر الإمكان. ثم العودة إلى المعنى الأصلي للأعضاء والنظر في الحل المهام لجميع القيم الممكنة للمعلمة. للقيام بذلك، تحتاج إلى تقسيم مجموعة قيم المعلمات إلى فترات زمنية.
4
عندما تبحث عن حدود فترات، وإيلاء الاهتمامعلى تلك التعبيرات التي تشارك فيها المعلمة. على سبيل المثال، لديك التعبير (أ -5)، بين حدود الفواصل يجب أن يكون هناك عدد من 5، لأن هذه القيمة تعكس القيمة بين قوسين إلى 0. التعبير مع المعلمة تحت علامة تقسيم، والجذر، وحدة، وما إلى ذلك من أهمية كبيرة.
5
عندما تجد كل الحدود الممكنةفترات، والنظر في وظيفتك لكل واحد منهم. لتبسيط هذه المهمة، ببساطة استبدال أحد الأرقام من هذه الفاصل الزمني في وظيفة وحل المشكلة. في كثير من الأحيان، ببساطة استبدال قيم مختلفة، يمكنك العثور على الطريق الصحيح لحل المشكلة.
نصيحة 6: الكتلة المولية: كيفية حساب
لحل مشاكل التصميم في معظم الحالاتمطلوب استخدام الكتلة المولية. إذا كانت الأوزان الذرية والجزيئية النسبية تحدد عادة من جدول العناصر الكيميائية ، D.I. Mendeleev دون مشاكل ، ثم مع الكتلة المولية ، في بعض الأحيان ، هناك صعوبات. ولكن في الواقع عدديًا تتطابق هاتان المعلمتان.

سوف تحتاج
- - النظام الدوري للعناصر الكيميائية مندليف
تعليمات
1
الجماهير الحقيقية للذرات صغيرة جدا ، وبالتاليستكون الحسابات ذات القيم التي تحتوي على عدد كبير من الأصفار صعبة للغاية. لذلك ، للراحة ، قدم مفهوم الشامة ، والتي يمكن في شكل أبسط أن تمثل كقطعة. وهذا ، إلى حد ما تبسيط مفهوم مفهوم الشامة ، يمكننا أن نفترض أن المواد تتفاعل مع بعضها البعض في نسب معينة جزء. و 1 حصة (أو 1 مول) من المادة لأي من المركبات لها نفس عدد الجزيئات أو الذرات أو الأيونات. هذه القيمة ثابتة وهي 6 ، 02 × 10 عند 23 درجة من أي جزيئات (رقم أفوجادرو). الكتلة المولية هي كتلة 1 مول من المادة ، يُشار إليها بالحرف M ولها وحدة قياس g / mole.
2
قبل الشروع في حساب الضرسكتلة، بالنسبة الذرية سابقا الحصول على (لذرات فردية) أو النسبية الجزيئية (الجزيئات) من الكتلة، والتي لا وحدة القياس (وحدة الكتلة الذرية لم تؤخذ في الاعتبار). للقيام بذلك ، ستحتاج بالتأكيد إلى مادة مرجعية - نظام دوري من العناصر الكيميائية DI. جامعة منديليف. يُسمح بهذا الجدول على جميع أنواع التحكم ، بما في ذلك الاستخدام في الكيمياء.
3
مثال رقم 1. حساب الضرس الوزن كلوريد الصوديوم. الحل. أولا ، تحديد الجزيئية النسبية الوزن (السيد) كلوريد الصوديوم (كلوريد الصوديوم) ، والذي يتألف منالكتلة الذرية النسبية (Ar) للصوديوم (Na) والوزن الذري النسبي (Ar) للكلور (Cl). Mr (NaCl) = Ar (Na) + Ar (Cl). Ar (Na) = 23 Ar (Cl) = 35.5 Mr (NaCl) = 23 + 35.5 = 58.5 اضرب النتيجة بـ 1 g / mol ، وهي الكتلة المولية لكلوريد الصوديوم (NaCl) .M (NaCl ) = 58.5 x 1 g / mol = 58.5 g / mol
4
مثال 2. حساب الضرس الوزن حمض orthophosphoric (H3PO4). الحل. أولاً ، حدد السيد (H3PO4) ، الذي يتكون من الكتل الذرية النسبية (Ar) للعناصر التي تشكل الجزيء. من الضروري أن نأخذ في الاعتبار حقيقة أن هناك 3 ذرات هيدروجين ، 1 ذرة فسفور و 4 ذرات أكسجين في الجزيء. لذلك ، السيد (H3PO4) = 3Ar (H) + Ar (P) + 4Ar (O) .3Ar (H) = 3 x 1 = 3 Ar (P) = 31 4Ar (O) = 4 x 16 = 64 Mr ( H3PO4) = 3 x 1 + 31 + 4 x 16 = 98 اضرب الناتج ب 1 g / mol ، الذي سيعطي الموليار الوزن حمض orthophosphoric (H3PO4) M (H3PO4) = 98 x 1 g / mol = 98 g / mol
نصيحة 7: كيف تتعلم كيفية حل المشاكل في الكيمياء
البرنامج المدرسي غني جدا،يتم اكتساب المعرفة النظرية، ولكن ليس هناك حل عملي. ما يجب القيام به وكيفية تعلم حل المشاكل في الكيمياء؟ ما هو المطلوب أولا من الطالب؟
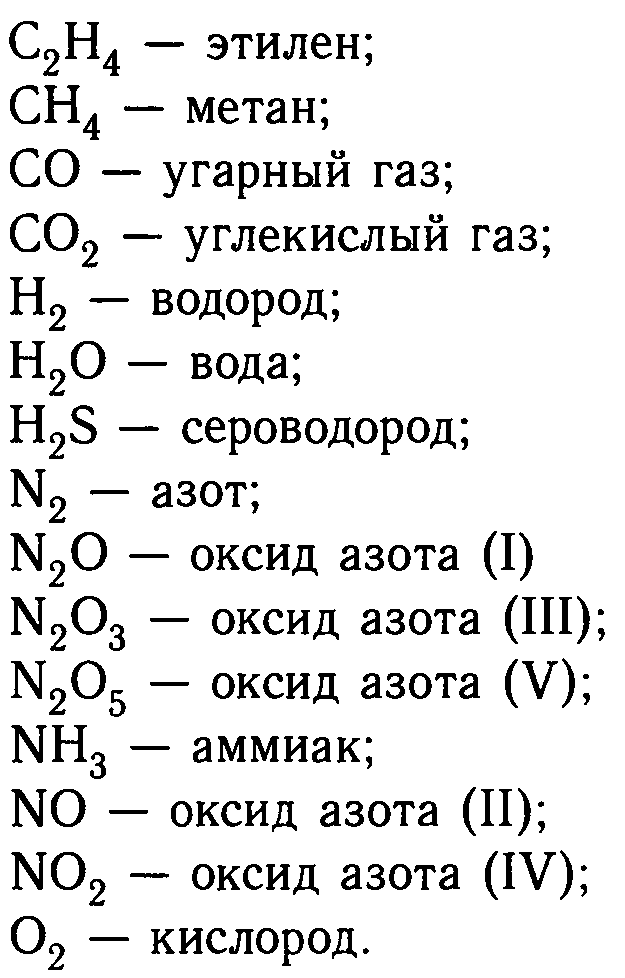
حل المشاكل في الكيمياء له تفاصيله الخاصة، وأنه من الضروري العثور على نقطة الانطلاق، والتي سوف تساعد على تعلم لفهم هذه المسألة الصعبة.
ما تحتاج إلى معرفته من أجل حل المشاكل في الكيمياء
لحل المشاكل في الكيمياء بشكل صحيح، في المقام الأولفمن الضروري أن نعرف ما هو تكافؤ العناصر. ذلك يعتمد على تركيبة صيغة المادة، ومعادلة التفاعل الكيميائي أيضا دون الأخذ بعين الاعتبار التكافؤ لا يتم تجميعها وتعادلها. يستخدم الجدول منديليف في كل مهمة تقريبا، تحتاج إلى معرفة كيفية استخدامه بشكل صحيح للحصول على المعلومات اللازمة عن العناصر الكيميائية، وكتلتها، والمستويات الإلكترونية. في معظم الأحيان في المهام المطلوبة لحساب كتلة أو حجم المنتج الناتج، وهذا هو الأساس.إذا لم يتم تحديد التكافؤ بشكل صحيح، فإن جميع الحسابات تكون غير صحيحة.ثم مهام أخرى أكثر تعقيدا، ستكونليتم حلها أسهل. ولكن أولا وقبل كل شيء - الصيغ من المواد والمعادلات وضعت بشكل صحيح من ردود الفعل الجارية، مشيرا إلى ما سوف تتحول في نهاية المطاف، وفي أي شكل. ويمكن أن يكون سائلا، أو غازا يتطور بحرية، أو مادة صلبة ترسب أو تذوب في ماء أو سائل آخر.
كيفية البدء عند حل المشاكل في الكيمياء
لحل المشكلة، يتم كتابة حالته لفترة وجيزة. بعد ذلك، يتم تجميع معادلة التفاعل. على سبيل المثال، يمكنك أن تنظر في البيانات المحددة: تحتاج إلى تحديد كتلة المادة التي تم الحصول عليها، كبريتيد الألومنيوم، في رد فعل من الألومنيوم المعدني مع حامض الكبريتيك، إذا أخذ الألومنيوم 2.7 غرام. إيلاء الاهتمام فقط للمادة التي هو معروف، بعد - لتلك التي تحتاج إلى العثور عليها. للبدء في حل من الضروري من نقل الوزن في غرام في المولي. تشكيل صيغة رد فعل، استبدال قيم الكتلة في ذلك وحساب نسبة. بعد حل مشكلة بسيطة، يمكنك أن تحاول أن تتعلم بشكل مستقل مماثلة، ولكن مع عناصر أخرى، وهذا ما يسمى، لملء يدك. الصيغ ستكون هي نفسها، فقط العناصر سوف تتغير. يتم تقليل جميع الحلول من المشاكل في الكيمياء لكتابة الصيغة الصحيحة للمادة، ثم إلى الصيغة الصحيحة لمعادلة التفاعل.يتم حل جميع المهام من خلال مبدأ واحد ، والشيء الرئيسي هو ترتيب معاملات بشكل صحيح في المعادلة.للتمارين يمكنك استخدام الإنترنت ، في ذلكعدد كبير من المهام المختلفة جدًا ، وبعد ذلك يمكنك رؤية خوارزمية الحل ، والتي يمكنك استخدامها بنفسك. وتتمثل الميزة في أنه يمكنك دائمًا مشاهدة الإجابة الصحيحة ، وإذا لم تتطابق النتيجة الخاصة بك ، فعليك أن تعرفها للعثور على الخطأ. يمكنك أيضًا استخدام الأدلة ومجموعات المهام للتدريب.







